Nicht-invasive Beatmung im Notfall: NIV richtig anwenden
NIV ist bei akuter respiratorischer Insuffizienz ein entscheidendes Werkzeug. Der Artikel erklärt Indikationen (COPD-Exazerbation, Lungenödem), Kontraindikationen, Geräteeinstellungen (CPAP vs. BiPAP), Monitoring und Abbruchkriterien.

Autor: Dr. med. univ. Daniel Pehböck, DESA
Facharzt für Anästhesiologie und Intensivmedizin, AHA-zertifizierter ACLS/PALS-Instructor, Kursleitung Simulation Tirol
Lesezeit ca. 8 Min.
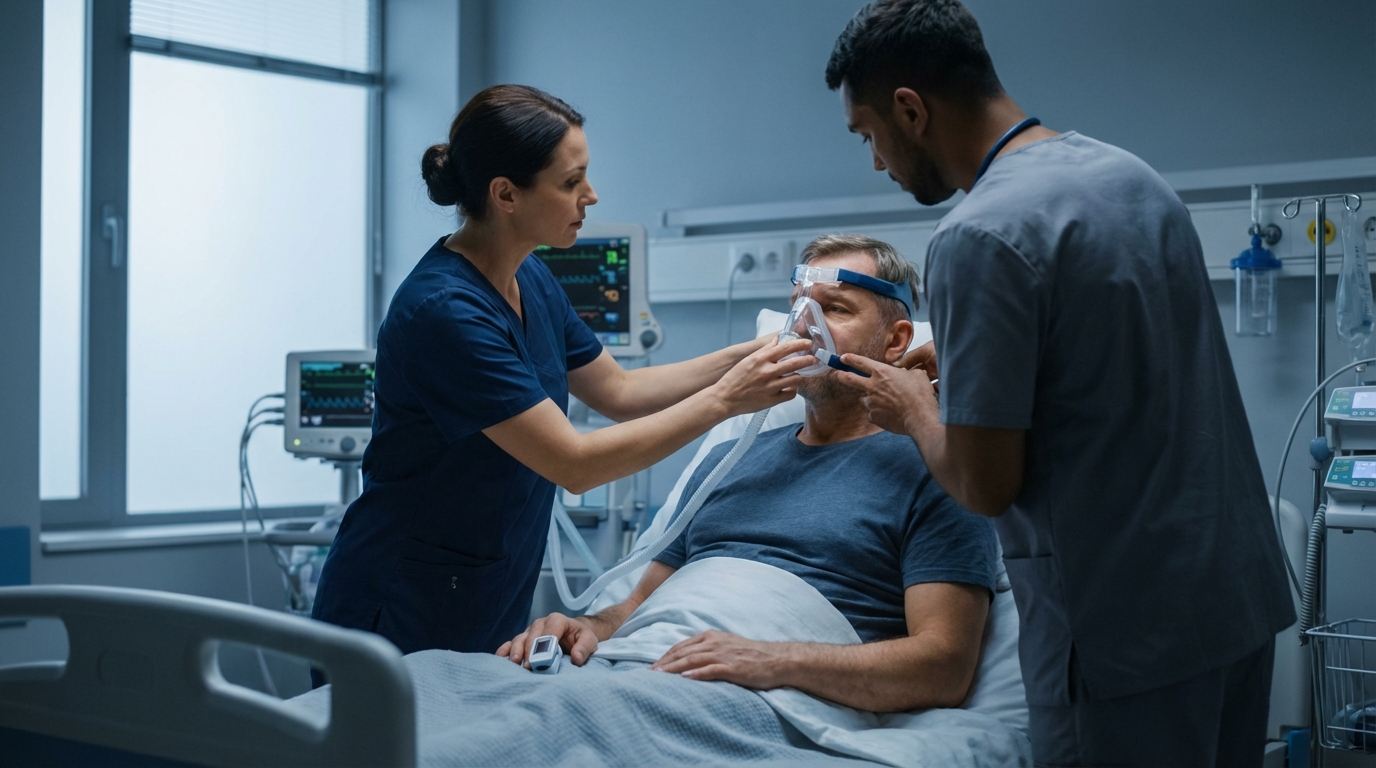
Die nicht-invasive Beatmung (NIV) gehört zu den wirksamsten Interventionen bei akuter respiratorischer Insuffizienz – und gleichzeitig zu jenen Maßnahmen, die im klinischen Alltag häufig zu spät, mit falschen Einstellungen oder bei ungeeigneten Patient:innen eingesetzt werden. Richtig angewandt senkt NIV die Intubationsrate, verkürzt den Intensivaufenthalt und reduziert die Mortalität bei ausgewählten Krankheitsbildern signifikant. Falsch angewandt verzögert sie eine notwendige Intubation und verschlechtert das Outcome. Dieser Artikel gibt dir einen praxisnahen Überblick über Indikationen, Kontraindikationen, Geräteeinstellungen, Monitoring und klare Abbruchkriterien – damit du im Notfall fundierte Entscheidungen treffen kannst.
Pathophysiologische Grundlagen: Warum NIV wirkt
Um NIV gezielt einzusetzen, lohnt sich ein kurzer Blick auf die zugrunde liegende Physiologie. Die akute respiratorische Insuffizienz lässt sich vereinfacht in zwei Typen unterteilen:
- Typ 1 (hypoxämisch): Oxygenierungsstörung bei normalem oder erniedrigtem pCO₂. Typische Ursache: alveoläres Lungenödem, Pneumonie, ARDS.
- Typ 2 (hyperkapnisch): Ventilationsstörung mit erhöhtem pCO₂ und respiratorischer Azidose. Typische Ursache: COPD-Exazerbation, neuromuskuläre Erschöpfung.
NIV wirkt über zwei zentrale Mechanismen:
- Positiver endexspiratorischer Druck (PEEP/EPAP): Hält Alveolen offen, rekrutiert atelektatische Lungenareale, reduziert intrapulmonalen Shunt und verbessert die Oxygenierung. Beim kardiogenen Lungenödem senkt der intrathorakale Druckanstieg zusätzlich die Vorlast und Nachlast des linken Ventrikels – ein therapeutisch erwünschter hämodynamischer Effekt.
- Inspiratorische Druckunterstützung (IPAP/PS): Reduziert die Atemarbeit, entlastet die erschöpfte Atemmuskulatur und verbessert das Tidalvolumen – entscheidend bei hyperkapnischem Versagen.
Das Verständnis dieser Mechanismen bestimmt, ob du CPAP oder BiPAP wählst und welche Drücke du einstellst.
Indikationen: Wann NIV einsetzen?
Die Evidenz für NIV ist nicht bei allen Formen der respiratorischen Insuffizienz gleich stark. Die beiden Hauptindikationen mit der besten Datenlage sind:
COPD-Exazerbation mit respiratorischer Azidose
Dies ist die Indikation mit der stärksten Evidenz. NIV reduziert hier nachweislich die Intubationsrate, die Mortalität und die Aufenthaltsdauer. Die Kriterien für den NIV-Einsatz sind:
- pH < 7,35 mit pCO₂ > 45 mmHg trotz optimierter medikamentöser Therapie (Bronchodilatatoren, Steroide, Sauerstoff)
- Klinische Zeichen der Atemerschöpfung: Tachypnoe > 24/min, Einsatz der Atemhilfsmuskulatur, paradoxe Atmung
- Erhaltenes Bewusstsein und kooperative:r Patient:in
Wichtig: Ein pH von 7,25–7,35 markiert den „Sweet Spot" für NIV bei COPD. Bei pH < 7,25 steigt das NIV-Versagerrisiko deutlich – hier solltest du NIV zwar versuchen, musst aber eine sehr niedrige Schwelle für die Intubation haben.
Akutes kardiogenes Lungenödem
Beim kardiogenen Lungenödem ist NIV neben Nitraten und Diuretika eine Erstlinientherapie. Die Mechanismen sind hier primär:
- Reduktion der Vorlast durch erhöhten intrathorakalen Druck
- Verbesserung der Oxygenierung durch alveoläre Rekrutierung
- Senkung der Nachlast des linken Ventrikels
Sowohl CPAP als auch BiPAP sind in dieser Indikation wirksam. Die Datenlage zeigt eine signifikante Reduktion der Intubationsrate und eine Verbesserung der klinischen Parameter innerhalb der ersten Stunde.
Weitere Indikationen
Mit geringerer Evidenz, aber klinisch vertretbar:
- Immunsupprimierte Patient:innen mit akuter hypoxämischer Insuffizienz (NIV als Brücke, um die Risiken einer invasiven Beatmung zu vermeiden)
- Postextubations-Versagen bei Risikopatient:innen
- Palliative Situation: NIV zur Symptomlinderung bei Dyspnoe, wenn eine Intubation nicht gewünscht ist
- Thoraxtrauma mit Rippenserienfraktur und erschwerter Atemmechanik
- Asthmaexazerbation: Hier ist die Evidenz schwächer, und du solltest eine sehr niedrige Schwelle für eine Eskalation beibehalten
Wann NIV bei hypoxämischer Insuffizienz ohne Lungenödem?
Beim De-novo-hypoxämischen Versagen (z. B. ambulant erworbene Pneumonie, ARDS) ist die Datenlage deutlich kritischer. Hier zeigen Studien, dass NIV die Intubation häufig nur verzögert, ohne das Outcome zu verbessern – mit dem Risiko, dass die Patient:innen zum Zeitpunkt der dann doch notwendigen Intubation in einem schlechteren Zustand sind. In dieser Situation verdient die High-Flow-Nasal-Cannula (HFNC) besondere Beachtung als Alternative.
Kontraindikationen: Wann NIV nicht anwenden
Absolute Kontraindikationen sind klar definiert und müssen vor jedem NIV-Versuch überprüft werden:
- Atemstillstand / Schnappatmung → sofortige Intubation
- Bewusstlosigkeit (GCS < 8) ohne rasch reversible Ursache → Aspirationsgefahr
- Fehlende Schutzreflexe → kein sicherer Atemweg
- Hämodynamische Instabilität (Schockindex > 1, therapierefraktäre Hypotension) → Intubation unter kontrollierten Bedingungen
- Gesichtstrauma / Gesichtschirurgie → Maske nicht adaptierbar
- Obere gastrointestinale Blutung oder aktives Erbrechen → Aspirationsrisiko
- Nicht drainierter Pneumothorax
Relative Kontraindikationen, die eine sorgfältige Nutzen-Risiko-Abwägung erfordern:
- Massive Sekretlast, die der/die Patient:in nicht abhusten kann
- Ausgeprägte Agitation oder Klaustrophobie
- Kürzliche Ösophagus- oder Magenoperation
- Schwere Hypoxämie mit SpO₂ < 85 % trotz maximaler FiO₂
CPAP vs. BiPAP: Die richtige Modalität wählen
Die Wahl zwischen CPAP und BiPAP ist keine Geschmacksfrage, sondern richtet sich nach der zugrunde liegenden Pathophysiologie.
CPAP (Continuous Positive Airway Pressure)
- Liefert einen konstanten Druck während In- und Exspiration
- Wirkt primär über alveoläre Rekrutierung und PEEP-Effekt
- Hauptindikation: Kardiogenes Lungenödem, rein hypoxämische Insuffizienz
- Vorteil: Einfach in der Anwendung, auch präklinisch mit Einwegsystemen (z. B. Boussignac-CPAP) verfügbar
- Starteinstellung: CPAP 5–10 cmH₂O, FiO₂ titrieren nach SpO₂-Ziel
BiPAP (Bilevel Positive Airway Pressure)
- Liefert zwei Druckniveaus: IPAP (inspiratorisch) und EPAP (exspiratorisch)
- Die Differenz IPAP – EPAP = Druckunterstützung (Pressure Support) entlastet die Atemmuskulatur und verbessert die Ventilation
- Hauptindikation: Hyperkapnisches Versagen (COPD-Exazerbation), gemischte Insuffizienz
- Starteinstellungen:
- EPAP: 4–6 cmH₂O
- IPAP: 10–14 cmH₂O (Druckunterstützung mindestens 5–6 cmH₂O über EPAP)
- FiO₂: Titrieren nach SpO₂ 88–92 % bei COPD, 92–96 % bei anderen Pathologien
- Atemfrequenz (Back-up): 12–16/min
Praxistipp zur Drucktitration
Starte mit moderaten Drücken und titriere in 2-cmH₂O-Schritten alle 5–10 Minuten nach oben, bis:
- Die Atemfrequenz sinkt (< 25/min)
- Der Einsatz der Atemhilfsmuskulatur nachlässt
- SpO₂ im Zielbereich liegt
- Der/die Patient:in subjektiv Erleichterung angibt
Maximale Drücke: IPAP sollte in der Regel 20–24 cmH₂O nicht überschreiten (Mageninsufflation, Leckage, Patientenkomfort). Falls diese Drücke nicht ausreichen, ist das ein Warnsignal für NIV-Versagen.
Maskenauswahl und Interface
Die beste Geräteeinstellung nützt wenig, wenn die Maske nicht passt. Die Maskenwahl ist ein unterschätzter Erfolgsfaktor:
- Oronasale Maske (Full-Face): Standardinterface im Notfall. Deckt Mund und Nase ab, verhindert Leckage bei Mundatmung. Nachteil: Aspirationsrisiko bei Erbrechen, Klaustrophobie.
- Nasenmaske: Besser toleriert, aber im Notfall bei Mundatmung ineffektiv.
- Totalface-Maske (Helm): Sehr gut toleriert, geringeres Druckstellenrisiko. Erfordert allerdings höhere Drücke und spezielle Geräte.
Praktische Tipps:
- Halte die Maske initial mit der Hand an, bevor du die Bänder fixierst – das gibt der/dem Patient:in Kontrolle und reduziert Angst
- Die Maske soll dicht sitzen, aber nicht zu fest: Zwei Finger sollten unter die Bänder passen
- Nasale Druckstellen entwickeln sich rasch – kontrolliere die Haut regelmäßig und verwende Hydrokolloiddressings prophylaktisch
Monitoring unter NIV: Was du im Auge behalten musst
NIV ist keine „Set-and-forget"-Therapie. Engmaschiges Monitoring in den ersten 30–60 Minuten entscheidet über Erfolg oder Abbruch.
Klinische Parameter (kontinuierlich)
- Atemfrequenz: Soll innerhalb von 30 Minuten sinken. Eine persistierende Tachypnoe > 30–35/min ist ein Warnsignal
- Atemanstrengung: Einsatz der Atemhilfsmuskulatur, Nasenflügeln, paradoxe abdominelle Atmung
- Bewusstseinslage: Zunehmende Somnolenz unter NIV ist ein Alarmzeichen
- Patientenkomfort: Agitation, Unruhe, Maskentoleranz
- Hämodynamik: Blutdruck, Herzfrequenz – hohe Drücke können die Vorlast kritisch senken
Apparatives Monitoring
- SpO₂: Kontinuierlich, Zielwert je nach Pathologie
- Blutgasanalyse (BGA): Entscheidend! Erste BGA nach 30–60 Minuten NIV. Verbesserung von pH und pCO₂ = beste Prädiktor:in für NIV-Erfolg
- Tidalvolumen: Falls am Gerät ablesbar – exzessive Tidalvolumina (> 9–10 ml/kg IBW) bei hypoxämischer Insuffizienz sind mit schlechtem Outcome assoziiert (sogenannte Patient Self-Inflicted Lung Injury, P-SILI)
- Leckage: Moderne Geräte zeigen die Leckage an – idealerweise < 25 l/min
Abbruchkriterien: Wann NIV scheitert
Der schwierigste Punkt bei NIV ist die Entscheidung zum Abbruch. Zu langes Zuwarten bei NIV-Versagen verschlechtert das Outcome der Patient:innen nachweislich. Folgende Kriterien sprechen für ein NIV-Versagen und die Notwendigkeit einer Intubation:
Frühes Versagen (< 1 Stunde)
- Keine Besserung oder Verschlechterung der Atemfrequenz
- Persistierende oder zunehmende Hypoxämie (SpO₂ < 88 % trotz FiO₂ > 0,6)
- Zunehmende Agitation oder abnehmende Vigilanz
- Hämodynamische Instabilität
- Intoleranz der Maske trotz optimierter Anpassung und milder Sedierung
Spätes Versagen (1–48 Stunden)
- Keine Verbesserung des pH-Wertes in der BGA nach 1–2 Stunden
- pCO₂ steigt weiter oder bleibt unverändert trotz optimierter Drücke
- Zunehmende Erschöpfung der/des Patient:in
- Neues Organversagen
Konkrete BGA-Kriterien für NIV-Versagen bei COPD
- pH nach 1 Stunde NIV weiterhin < 7,25 → hohe Versagerrate, Intubation erwägen
- pH nach 1 Stunde NIV < 7,30 und keine Besserungstendenz → intensiviertes Monitoring, Intubationsbereitschaft
- pH nach 1 Stunde NIV ≥ 7,30 mit Besserungstendenz → NIV fortsetzen, nächste BGA nach 2–4 Stunden
Merke: Definiere den Zeitpunkt der Reevaluation bereits bei NIV-Start. Kommuniziere im Team: „Wir machen jetzt einen NIV-Versuch. BGA-Kontrolle in 30 Minuten. Wenn sich der pH nicht bessert, intubieren wir." Diese proaktive Planung verhindert die gefährliche Trägheit des „Noch ein bisschen abwarten."
Sedierung unter NIV
Milde Sedierung kann die Maskentoleranz verbessern, muss aber sehr vorsichtig dosiert werden, da Atemdepression das NIV-Versagen beschleunigt:
- Dexmedetomidin: Mittel der Wahl auf der Intensivstation. Geringe Atemdepression, gute anxiolytische Wirkung. Dosierung: 0,2–0,7 µg/kg/h als Dauerinfusion.
- Morphin: In niedriger Dosierung (1–2 mg IV titriert) beim kardiogenen Lungenödem zur Reduktion der sympathoadrenergen Stressantwort und Dyspnoe. Cave: Atemdepression.
- Benzodiazepine: Im Notfall bei NIV grundsätzlich vermeiden – hohes Risiko der Atemdepression und paradoxen Agitation.
Häufige Fehler in der Praxis
Die folgenden Fehler sehen wir in der Praxis regelmäßig – und sie sind vermeidbar:
- Zu spätes Beginnen: NIV bei COPD-Exazerbation erst nach Stunden im Schockraum statt bereits bei Eintreffen. Je früher NIV beginnt, desto besser das Outcome.
- Zu niedrige Drücke: IPAP von 8 cmH₂O über EPAP von 4 cmH₂O liefert eine Druckunterstützung von nur 4 cmH₂O – das ist in der akuten Situation meist zu wenig.
- Falsche Modalität: CPAP bei einem hyperkapnischen COPD-Patienten ohne inspiratorische Druckunterstützung verbessert die Ventilation nicht ausreichend.
- Kein klarer Abbruchzeitpunkt: NIV wird stundenlang fortgesetzt, obwohl klinisch keine Besserung eintritt – die Intubation erfolgt dann unter deutlich schlechteren Bedingungen.
- Fehlende BGA-Kontrolle: Ohne BGA nach 30–60 Minuten fehlt die objektive Grundlage für die Entscheidung.
- Vernachlässigung der Grundtherapie: NIV ersetzt nicht Bronchodilatatoren, Steroide, Nitrate oder Diuretika – sie ist ein Add-on.
Zusammenfassung: NIV-Algorithmus im Notfall
- Indikation prüfen: COPD-Exazerbation mit pH < 7,35? Kardiogenes Lungenödem? → NIV indiziert
- Kontraindikationen ausschließen: Bewusstsein? Schutzreflexe? Hämodynamik?
- Modalität wählen: Hyperkapnie → BiPAP. Reines Oxygenierungsproblem → CPAP (oder BiPAP)
- Interface anlegen: Oronasale Maske, initial mit Hand halten, Patient:in beruhigen
- Startdrücke: EPAP 5 cmH₂O, IPAP 10–12 cmH₂O, FiO₂ nach Bedarf
- Titrieren: Alle 5–10 Minuten um 2 cmH₂O nach Klinik
- BGA nach 30–60 Minuten: pH verbessert? pCO₂ rückläufig? → Weiter. Nicht verbessert? → Intubationsbereitschaft
- Engmaschiges Monitoring: Atemfrequenz, SpO₂, Vigilanz, Hämodynamik
- Abbruchkriterien einhalten: Lieber eine geplante Intubation zu früh als eine Notintubation zu spät
Praktisches Training
Die nicht-invasive Beatmung im Notfall ist eine Maßnahme, die unter Zeitdruck, bei unkooperativen Patient:innen und mit komplexen Entscheidungspfaden funktionieren muss. Geräteeinstellungen, Maskenwahl, Drucktitration und die kritische Entscheidung zwischen Fortführen und Intubation lassen sich am besten in realistischen Simulationsszenarien trainieren. In unseren Notfalltrainings bei Simulation Tirol übst du genau diese Situationen hands-on – von der Erstanlage über das Troubleshooting bei Leckage bis zur strukturierten Reevaluation. Mehr Informationen findest du unter simulation.tirol/kurse/notfalltraining.
Du willst das praktisch trainieren?
In unserem Notfalltraining in deiner Arztpraxis oder Klinik übst du dieses Thema hands-on mit High-Tech-Simulatoren und erfahrenen Instruktor:innen.
Weitere Artikel
Akute Atemnot: Differenzialdiagnose und Soforttherapie
Dyspnoe hat zahlreiche Ursachen von Asthma über Herzinsuffizienz bis zur Lungenembolie. Der Artikel stellt einen systematischen Approach zur Differenzierung anhand von Anamnese, Klinik, Auskultation und Point-of-Care-Diagnostik vor.
Akute Hypoglykämie: Notfalltherapie bei Erwachsenen und Kindern
Grenzwerte, Symptomerkennung, orale Glukosegabe vs. i.v.-Dextrose vs. Glukagon – mit separaten Dosierungen für Erwachsene und pädiatrische Patienten. Ein häufiges Notfallbild systematisch aufbereitet.
Akute Nebenniereninsuffizienz: Addison-Krise im Notfall
Die adrenale Krise wird häufig verkannt und kann tödlich enden. Der Artikel beschreibt Risikopatienten, klinische Zeichen, die sofortige Hydrocortison-Gabe und das Management begleitender Hypoglykämie und Hyperkaliämie.

